Compiti di termodinamica per la 5 classico anno 2012 – 2013
2 marzo 2013 ( su richiesta di Conti).
compiti 5Class ( apri il file)

Sadi Carnot (Parigi1 giugno1796 – Parigi 24 agosto1832) fisico e ingegnere francese, è considerato uno dei padri fondatori della termodinamica.
Ciclo di Carnot: due isoterme e due adiabatiche. (massimo rendimento della macchina che lavora fra due temperature, T1 e T2, T2 > T1).
Si dimostra che per il ciclo di Carnot, il rendimento è :
h = (T2 – T1)/T2 < 1 .
I principi della termodinamica:
1° Principio della termodinamica.
In una trasformazione termodinamica la quantità di calore totale scambiato da un sistema, si trasforma parte in lavoro e parte in variazione dell’energia interna del sistema. Questo principio ci dice che l’energia si conserva; ma essendo il calore una forma di energia cinetica disordinata, non tutto il calore diventa lavoro meccanico; una parte fa variare l’energia interna del sistema.
In formula : Q = L+ DeltaU.
U è detta energia interna, è in pratica energia cinetica molecolare ed è una funzione di stato, dipende cioè solo dallo stato in cui si trova il sistema, la sua variazione DeltaU dipende solo dalla variazione di temperatura.
DeltaU = Q – L .
2° Principio della termodinamica.
Enunciato di Kelvin Planck:
E’ impossibile realizzare una trasformazione ciclica il cui unico risultato sia quello di sottrarre calore ad un’unica sorgente e trasformarlo integralmente in lavoro meccanico. (occorrono sempre almeno due sorgenti a diversa temperatura.
Enunciato di Clausius:
E’ impossibile realizzare una trasformazione il cui unico risultato sia quello di far passare il calore da una sorgente a temperatura T1 ad un’altra a temperatura T2 > T1. ( Il calore fluisce spontaneamente da un corpo a temperatura maggiore a un corpo a temperatura inferiore; per ottenere il passaggio contrario, occorre spendere energia, fare lavoro). Questo si ottiene con una macchina frigorifera che spendendo energia, preleva calore dalla cella frigorifera a temperatura bassa e lo cede all’ambiente esterno a temperatura più alta, mantenendo freddo l’ambiente dentro il frigorifero).
I principi della termodinamica (Power point)
Lavoro in una trasformazione termodinamica
Se un gas perfetto (sistema termodinamico) viene fatto espandere in un cilindro
munito di pistone capace di muoversi, il gas compie lavoro. Occorre considerare una situazione ideale dove la trasformazione subìta dal gas sia “quasi statica”, cioè passi per stati successivi di equilibrio, dei quali sono noti sempre Pressione, Volume e Temperatura. La trasformazione viene detta reversibile perché può essere percorsa anche in senso inverso per riportare il gas nello stato iniziale.
Le tre coordinate sono in relazione nell’equazione PV = nRT.
Riportando nel piano P-V, l’andamento della pressione in funzione del volume, il lavoro è rappresentato dall’area sottostante il grafico, fino all’asse dei volumi. E’ positivo se VB >VA, è negativo se VB < VA .
http://www.ripmat.it/mate/c/ck/cke.html : (che cosa è un integrale)


Isoterma : Q = L
Un palloncino è riempito di 6 litri a pressione atmosferica. Viene immerso in una piscina, di temperatura costante e pari a quella dell’aria (20°). se il volume finale è di 2,91 litri, a che profondità è stato immerso?
Isoterma, T = costante; Po = 1 atmosfera = 1,013 * 10^5 Pa
P1 * V1 = Po * Vo; il volume diminuisce, la pressione aumenta.
P1 = Po * Vo / V1 = 1 * 6 / 2,91 = 2,062 atmosfere
P1 = 2,062 * 1,013 * 10^5 Pa = 2,089 * 10^5 Pa
Legge di Stevino:
P = Po + densità * g * h
densità acqua = 1000 kg/m^3
h = (P – Po) / (densità * g)
h = (2,089 – 1,013) * 10^5 /(1000 * 9,8) = 1,076 * 10^5 / 9800 = 10,98 m = 11 m

isobara:
Q = L + ΔU

isocora : Q = ΔU; L = 0
 isoterma
isoterma
isoterma: PV = costante
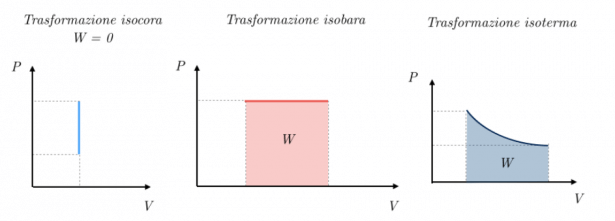
Confronto fra trasformazioni : il lavoro è rappresentato dall’area sottostante il grafico.
Leggi dei gas perfetti. Per gas perfetto si intende un aeriforme perfettamente comprimibile, i cui atomi o molecole possono essere considerati punti materiali che interagiscono fra loro solo mediante urti totalmente elastici dove si conserva l’energia cinetica delle particelle.
Per descrivere lo stato di un gas (cioè un sistema termodinamico) occorre conoscere il valore delle coordinate termodinamiche: pressione P, volume V, temperatura assoluta T. Un gas compie una trasformazione termodinamica quando modifica il proprio stato (cambiano le coordinate).
Prima legge di Gay-Lussac, isobara : P costante.
V = Vo ( 1+ α * t ) , P costante, (legge delle isobare).
α = 1/273,15 °C-1 coefficiente di dilatazione dei gas. Vo : volume a 0°C;
Seconda legge di Gay-Lussac, isocore: V costante.
P = Po ( 1+ α * t ) , α = 1/273,15 °C-1
Cambiando la scala delle temperature da °C a Kelvin,
T = t + 273,15 le due leggi di Gay-Lussac diventano:
V = Vo α T ; P = Po α T ;
diretta proporzionalità con T (assoluta).
Prima legge di Gay-Lussac, isobara : P costante.
V2 / T2 = V1 / T1; V e T sono direttamente proporzionali.
Seconda legge di Gay-Lussac, isocore: V costante.
P1 / T1 = P2 / T2; P e T sono direttamente proporzionali.
Legge di Boyle, isoterme P * V = Po * Vo;
P * V = costante, T costante.
Vo e Po, volume e pressione a 0°C = 273 K.
Lavoro nell’isoterma: L = n R T ln(V1/Vo).
Esempio: Una massa di 10 g di idrogeno si espande reversibilmente secondo la legge PV=K; con K=13,4 Litri atm, da una pressione P1=5,4 atm ad una pressione P2 =2,6 atm.
Calcolare il lavoro compiuto dal gas.
L’idrogeno è biatomico (H2); la sua massa molare è:
MM = 2 grammi/mol;
La trasformazione è isoterma:
P * V = costante;
P * V = 13,4 L atm; (abbiamo come unità di misura litri e atmosfere, quindi come costante dei gas perfetti si usa:
R = 0,082 (Litri atm/molK);
P1 = 5,4 atm;
V1 = 13,4/5,4 = 2,48 Litri
P2 = 2,6 atm;
V2 = 13,4 / 2,6 = 5,15 Litri. Il gas si espande e fa lavoro
n = massa / MM = 10 / 2 = 5 mol;
Occorre la temperatura T.
R = 0,082 (L atm/molK);
PV = n R T;
T = PV / nR = 13,4 / (5 * 0,082) = 32,7 K
Lavoro isoterma è l’area sottostante il grafico dell’iperbole PV = K;
Se vogliamo il lavoro in Joule, R deve essere:
R = 8,31 J/molK.
L= nRT ln(V2/V1);
L = 5 * 8,31 * 32,7 * ln(5,15 / 2,48) = 5 * 8,31 * 32,7 * ln(2,077);
L = 1358,68 * 0,731 = 993 J.

A -> B isobara;
DeltaU = cv n (Tb – Ta) = (3/2 R)* 1* (800 – 400) = 12,465 * 400 =
= + 4986 J.
L = P * (DeltaV); Per la legge dei gas perfetti : P * DeltaV = n R DeltaT
L = 1 * 8,31 * 400 = 3324 J ; Q = L + DeltaU = (cp n DeltaT) = 8310 J .
B -> C isocora; DeltaU = cv n DeltaT = 3/2R * 1* (400 – 800) = – 4986 J;
L = 0 J; Q = DeltaU = – 4986 J.
C -> D isobara; DeltaU = cv n (Td – Tc) = (3/2 R) * 1* (200 – 400) = 12,465 * (- 200) = – 2493 J. L = P * (DeltaV) = n R * DeltaT = 1 * 8,31 * (200 – 400) = – 1662 J ;
Q = L + DeltaU = – 2439 – 1662 = – 4101 J.
D -> A isocora, DeltaU = cv n DeltaT = 3/2R * 1* (800 – 200);
DeltaU = 12,465 * 600 = 7479 J; L = 0 J; Q = DeltaU = + 7479 J.
R= 8,31 J /(molK); costante dei gas perfetti.
cv = calore specifico a volume costante = 3/2 R = 12,465 J/(molK);
cp = calore specifico a pressione costante.
cp = cv + R = 5/2 R = 20,775 J / (molK).
Adiabatica: Q = 0 ; L = – ΔU

adiabatica: senza scambi di calore con l’ambiente esterno. Q = 0. Il lavoro viene fatto a spese dell’energia interna del gas.
( In questo grafico: P diminuisce, V aumenta, la temperatura T diminuisce).
P * V^(cp/cv) = costante
Una trasformazione adiabatica è una trasformazione termodinamica nel corso della quale un sistema fisico non scambia calore con l’ambiente esterno. Il termine deriva dal greco ἀ- (“alfa privativo”), διὰ- (“attraverso”), e βαῖνειν (“passare”) e significa quindi “che non permette di passare attraverso”.
Equazioni di Poisson dell’adiabatica reversibile
- P * (V^gamma) = costante
- T * (V ^ (gamma-1) ) = costante
dove gamma = Cp / Cv e Cp = Cv + R
gamma è l’esponente da dare al volume:
Per un gas monoatomico: gamma = cp/cv = (5/2 R) / (3/2R) = 5/3
Per un gas biatomico: gamma = cp/cv = (7/2 R) / (5/2R) = 7/5
Po * (Vo)^5/3 = P1 * (V1)^5/3
Per un gas poliatomico:
cp = 4 R; cv = 3 R; cp / cv = 4/3
Esercizi – Lavoro
1) Un gas, contenuto in un cilindro munito di stantuffo, occupa a pressione normale il volume di 1,0 l. Riscaldato a pressione costante il gas si espande molto lentamente fino a raddoppiare il suo volume. Qual è il lavoro compiuto a seguito dell’espansione?
A=1 J
B=20 J
C=100 J
D=200 J
1) L = P * Delta V = 1,013 * 10^5 Pa x ( 2 – 1) * 10^-3 m^3 = 100 J circa
risposta C
2) Alla pressione di 100 kPa un gas si espande in modo reversibile dal volume di 1,40 m^3 al volume di 2,75 m^3. Calcola il lavoro compiuto dal gas.
L = 100000 * ( 2,75 – 1,40) = 1,35 * 10^5 J = 135 * 10^3 = 135 kJ
3) Un gas occupa inizialmente un volume di 9,2 dm^3 e viene lentamente compresso a pressione atmosferica mediante un lavoro pari a 510 J. Qual è il volume finale del gas?
DeltaV = L / P; il lavoro è negativo perchè è fatto dall’esterno sul gas.
Vfin – Vo = – 510 /1,013 * 10^5 = 5,03 * 10^-3 m^3 = – 5,0 dm^3
Vfin – 9,2 = – 5,0
Vfin = – 5,0 + 9,2 = 4,2 dm^3
3 bis) isobara:
Un gas ha una temperatura iniziale di 0°C. Il gas viene riscaldato a pressione costante fino a quando il suo volume è aumentato di un decimo. Calcolare la temperatura finale del gas.
V1/ T1 = Vo / To; ( Legge delle isobare V e T sono direttamente proporzionali, P è costante- Legge di Charles).
To = 0° + 273 = 273 K
V1 = Vo + 1/10 * Vo = Vo * (1 + 1/10)
Vo * (1 + 1/10) / T1 = Vo / 273;
Vo si semplifica.
(1 + 1/10) / T1 = 1 / 273;
T1 / (1 + 1/10) = 273
T1 = 273 * (11/10) = 300 K
T1 in °C = 300 – 273 = 27°C
4) Ciclo: isocora, adiabatica, isobara.
Una quantità di gas elio pari a n= 0.1mol subisce un ciclo termodinamico costituito da una sequenza di tre trasformazioni: una isocora (1→2), un’adiabatica (2→3) ed un’isobara (3→1).
Nello stato 1 volume e temperatura sono rispettivamente V1= 1 litro e T1= 300 K; nello stato 2 la temperatura è T2= 600 K.
a. Disegnare nel piano PV il ciclo descritto.
b. Si calcoli il rendimento del ciclo nell’ipotesi che tutte le trasformazioni siano perfettamente reversibli e che il gas si possa considerare ideale.
P1 = n R T1/ V1= 0,1 * 0,082 * 300 /1 = 2,46 atm
P2/T2 = P1/T1
P2 = 2,46 * 2 = 4,92 atm
V2 = 1 litro
P3 = P1 = 2,46 atm perchè la trasformazione finale deve essere isobara e tornare allo stato 1.
adiabatica: P2 * (V2^5/3) = P3 * ( V3^5/3)
V3^5/3 = (P2/P3) * V2^5/3
V3 = V2 * (P2/P3)^3/5 = 1 * (4,92/2,46)^3/5
V3 = 1 * 2^3/5 = 1,52 litri
T3 = P3 * V3/ nR = 2,46 * 1,52/(0,1 x 0,082) = 455 K
Lavoro nell’isocora = 0 J
Lavoro nell’adiabatica L = – ΔU; L (2–>3) = – 3/2 R * n * ( T3 – T2)
L (2–>3) = – 3/2 * 8,31 * 0,1 * ( 455 – 600) = + 180,7 J
Lavoro isobara L (3–>1) = P1 * (V1 – V3) = 2,46 * ( 1 – 1,52) = – 1,28 litri atm
Lavoro in Joule L (3–>1) = – 1,28 * 1,013 * 10^5 Pa * 10^-3 m^3 = – 130 J
Lavoro utile = 180,7 – 130 = 50,7 J
Calore assorbito nell’isocora: Q (1–>2) = Cv * n * (T2 – T1) =
= 3/2 * 8,31 * 0,1 * (600 – 300)
Q (1–>2) = 374 J (calore assorbito);
nell’adiabatica Q = 0; (
nell’isobara il calore viene ceduto).
rendimento eta = L utile / Qass
eta = 50,7/ 374 = 0,14 = 14%
grafico: isocora, linea verticale; adiabatica, un’iperbole più calante; isobara, linea orizzontale che chiude la figura, una specie di triangolino rettangolo che ha per ipotenusa la curva dell’adiabatica.
5) Ciclo isobara, isocora, adiabatica
7 Moli di un gas perfetto monoatomico, inizialmente nello stato 1 caratterizzato dalla pressione P1 e dal volume V1, compie un ciclo reversibile costituita da una isobara 1-2, che conduce al volume V2 = 8 V1, dalla trasformazione isocora 2-3 che porta alla pressione P3 = 1/12 P1 e dalla compressione adiabatica 3-1. Il rendimento è: A) 0,05 B) 0,75 C) 0,43 D) 0,79 E)0,37.
Per un gas perfetto monoatomico il calore specifico è :
cv = (3/2)R ; (a volume costante)
cp = (5/2)R ; ( a pressione costante).
n = 7 mol.
Nell’isobara 1-2 il gas assorbe calore:
Qass = cp n ( T2 – T1)
P1 V1 = nRT1;
T1 = P1 V1 / nR
P2 V2 = n R T2
P1 * 8 V1 = n R T2
T2 = P1 * 8 V1 / n R
Q assorbito = = 5/2 R * n* [P1 * 8 V1 / n R – P1 V1 / nR ] =
= 5/2 * (8 – 1) * P1 * V1 = 35/2 * P1 V1.
Qass = 17,5 * P1 V1.
Isocora: Q ceduto = 3/2 R n ( T3 – T2)
P3 V3 = 1/12 P1 * 8 V1 = 8 / 12 * P1V1=
P3 V3 =(2/3) P1 V1
T3 = P3 V3 / nR = 2/3 P1 V1 / nR;
Q ceduto = 3/2 R n ( T3 – T2) = 3/2 R n * ( 2/3 * P1 V1 / nR – P1 * 8 V1 / n R)
Q ceduto = 3/2 * P1 V1* (2/3 – 8);
Q ceduto = 3/2 * (-22/3) * P1 * V1 = – 11 P1 * V1; (è negativo perché ceduto).
Adiabatica: Q = 0 J;
rendimento r = ( Qass – |Qced|) / Qass;
r = ( 17,5 * P1 V1 – 11 P1 * V1) / (17,5 * P1 V1);
P1 V1 si semplifica e resta:
r = ( 17,5 – 11) / 17,5 = 0,37
risposta E.


Ciclo di Carnot. isoterma, adiabatica, isoterma, adiabatica.
Esercizio : Una mole di gas perfetto monoatomico compie un ciclo di Carnot
A-B-C-D tra le temperature T2= 700 °C e T1 = 20 °C. II volume iniziale è VA = 30 litri mentre VB = 60 litri. Calcolare:
1. i volumi VC e VD;
2. il lavoro effettuato in un ciclo.
T1 = 700 + 273 = 973 K; T2 = 20 + 273 = 293 K
rendimento eta = (T2 – T1) / T2 = 973 – 293/973 = 680/973 = 0,7 = 70%
1. Qassorbito da A a B = Lavoro isoterma = nRT2 ln(VB/VA) =
= 1 x 8,31 x 973 ln(60/30) = 5605 J
eta = (Lavoro ciclo)/ Qassorbito
(Lavoro ciclo) = eta x Qassorbito = 0,7 x 5605 = 3923 J
2.Qceduto = 5605 – 3923 = 1682 J
Qceduto è pari al lavoro della isoterma da C a D
LCD = nRT1 ln(VD/VC) = – 1682
ln(VD/VC) = -1682/(1 x 8,31 x 293) = – 0,691
VD/VC = 0,5
TB x VB^(5/3-1) = TC x VC^(5/3-1) (equazione dell’adiabatica)
VC = (973 x 60^(2/3)/293)^ (3/2) = (973/293)^(3/2) x 60 =
= 6,05 x 60 = 363 litri
VD = 0,5 x 363 = 181,5 litri.
Esempio isoterma: Un subacqueo in immersione emette una bolla d’acqua che quando raggiunge la superficie ha raddoppiato il suo volume. Facciamo l’ipotesi che la temperatura si mantenga costante. A che profondità si trova il subacqueo ?
[10,3 m]
P1 x V1 = P2 x V2 (isoterma)
V2 = 2 V1; P2 = P atmosferica in superficie
P1 x V1 = P2 x 2 x V1; semplificando V1, rimane:
P1 = 2 P2 = 2 atmosfere
Legge di Stevin.
(ro) g h + Po = 2 atmosfere;
(ro) g h = 1 atmosfera = 1,013 x 10^5 Pa
1000 x 9,8 x h = 1,013 x 10^5; ro = 1000 kg/m^3 densità dell’acqua.
h = 1,013 x10^5 /(1000 x 9,8) = 10,3 m; ogni 10 metri circa la pressione aumenta di un’atmosfera.
Primo principio della termodinamica. In una trasformazione termodinamica la quantità di calore totale scambiato da un sistema, si trasforma parte in lavoro e parte in variazione dell’energia interna del sistema. Questo principio ci dice che l’energia si conserva, ma essendo il calore una forma di energia cinetica disordinata, non tutto il calore diventa lavoro meccanico; una parte fa variare
l’energia interna del sistema. In formula : Q = L + DU.
U è dettaenergia interna, è in pratica energia cinetica molecolare ed è una funzione di stato, dipende cioè solo dallo stato in cui si trova il sistema, la sua variazione DU dipende solo dalla variazione di temperatura.
DU = Q – L
Calore specifico di un gas perfetto. Per un gas occorre definire due tipi di calore specifico: cp a pressione costante, cv a volume costante (cp > cv). A pressione costante un gas assorbe maggiore quantità di calore piuttosto che a volume costante .
In una isocora L = 0; Q = DU; Q = 3/2 nRDT; Q = cv n DT quindi
cv = 3/2 R = 12,47 J/molK, calore specifico molare, calore che
occorre per scaldare una mole di un gas monoatomico di un grado centigrado a volume costante.
In una isobara Q = L+ DU; Q = P DV + 3/2 n RDT;
essendo per la legge dei gas: PDV = n R DT allora
Q = nRDT + 3/2 n RDT; per cui Q = n DT ( R + 3/2 R);
ponendo R + 3/2 R = 5/2 R = cp; Q = cp nDt.
cp = cv + R ( equazione di Mayer); cp è il calore che occorre per scaldare una mole di gas di un grado a pressione costante;
si misura in Joule /(mol K).
Per un gas biatomico cv = 5/2 R ; cp = 7/2 R
Esercizio: Una mole di gas ossigeno O2 cambia il proprio stato termodinamico mediante una trasformazione isobara che fa variare di un fattore 3 il volume del gas. Sapendo che il gas si trova inizialmente alla pressione atmosferica ed alla temperatura di 27°C, calcolare la variazione di energia interna.
[R: ∆U = 12465 J]
In una isobara Q = L + DeltaU,
una parte di calore non fa lavoro, ma fa aumentare l’agitazione molecolare e quindi l’energia interna U.
Delta U = Cv x n x ( Tfin – To)
Cv è il calore specifico molare a volume costante. Per un gas biatomico vale 5/2 x R
Bisogna trovare Tfinale
Legge delle isobare:
V1/T1 = Vo/To; V1 = 3 x Vo;
3 Vo / T1 = Vo /To
T1 = 3 Vo x To / Vo = 3 x To
Volume e temperatura assoluta sono direttamente proporzionali: se il volume triplica, anche la temperatura triplica.
To = 27° + 273 = 300 K
T1 = 300 x 3 = 900 K
deltaU = 5/2 x 8,31 x 1 x ( 900 – 300) = 12465 J
Secondo principio della termodinamica.
Enunciato di Kelvin Planck: E’ impossibile realizzare una trasformazione ciclica il cui unico risultato sia quello di sottrarre calore ad un’unica sorgente e trasformarlo integralmente in lavoro meccanico. (Occorrono sempre almeno due sorgenti a diversa temperatura.

Una macchina termica preleva calore Q2 dalla sorgente calda a temperatura T2, fa lavoro L e cede calore Q1 alla sorgente fredda a temperatura T1.
L = Q2 – Q1

ciclo termodinamico:
il lavoro è rappresentato dall’area racchiusa dal grafico.
Enunciato di Clausius: E’ impossibile realizzare una trasformazione il cui unico risultato sia quello di far passare il calore da una sorgente a temperatura T1 ad un’altra a temperatura T2 > T1.
(Il calore fluisce spontaneamente da un corpo a temperatura maggiore a un corpo a temperatura inferiore;
per ottenere il passaggio contrario, occorre spendere energia, fare lavoro. Questo si ottiene con una macchina frigorifera che spendendo energia, preleva calore dalla cella frigorifera a temperatura bassa e lo cede all’ambiente esterno a temperatura più alta, mantenendo freddo l’ambiente dentro il frigorifero).
Sadi Carnot
Teorema di Carnot: Nessuna macchina irreversibile (reale), può avere un rendimento maggiore di una macchina reversibile (ideale),
che lavora tra le stesse sorgenti della macchina reale. Il rendimento di una macchina ideale (di Carnot), dipende solo dalle temperature assolute a cui si trovano le due sorgenti. Il ciclo di Carnot è costituito da due trasformazioni isoterme e da due trasformazioni adiabatiche, ed ha il rendimento massimo. Il rendimento è dato da:
η = L / Q2 = (Q2 – Q1) /Q2 < 1
(Q2 : calore assorbito dalla sorgente calda,
Q1 : calore ceduto alla sorgente fredda che non diventa lavoro meccanico).
Si dimostra che per il ciclo di Carnot, il rendimento è :
h = (T2 – T1)/T2 < 1 .

Ciclo di Carnot: due isoterme e due adiabatiche
Quesito 1: Una macchina ideale lavora tra le temperature di 700K e 300K. Calcola il rendimento. Calcola il lavoro fatto quando la quantità di calore assorbito è Q = 15000 J. Calcolare la potenza, sapendo che la macchina compie 15 cicli al minuto.
( rendimento eta) h= (700-300) / 700 = 0,57 = 57% (rendimento)
L/Q = h
L = 0,57 x 15000= 8550 J
Potenza = lavoro/tempo
Potenza = L/t = 15 x 8550 /(60 s) = 2138 W
Potenza = 2,14 kW
Quesito 2 : Può esistere una macchina termica che in un ciclo assorba la quantità di calore Qa =1000 J da una sorgente a temperatura Tmax= 900 K e ceda una quantità di calore di Qc= 500 J ad una sorgente di Tmin=600 K?
Avrebbe un rendimento eta pari a L /Qa
eta = (Qa – Qc) / Qa = =(1000 – 500) /1000 = 0,5 = 50%
Ma una macchina termica reale non può avere rendimento >di quello della macchina di Carnot.
h(Carnot) = (T2 – T1) / T2 = (900 – 600) / 900 = 0,33 = 33%
Non può esistere.
Quesito 3 : In un motore diesel la combustione del carburante è provocata dal riscaldamento dell’aria dovuto alla compressione. Nel cilindro il gas si trova inizialmente alla temperatura di 305 K e poi è compresso in un volume che è 1/16 di quello iniziale e a una pressione che è 48 volte la pressione iniziale.
Determina la temperatura del gas dopo la compressione.
V2 = 1/16 V1
P2 = 48 P1
T1 = 305 K
P1 x V1 /T1 = P2 x V2/T2
T2 =P2 x V2 x T1 / (P1 x V1)
T2 = 48 P1 x 1/16 V1 x 305/ (P1 x V1); P1 x V1 si semplifica.
T2 = 48 x 1/16 x 305 = 3 x 305 = 915 K
2° principio – Entropia: Si definisce “variazione di entropia” in una trasformazione termodinamica: DS = SQ/T
la somma di tutti i calori scambiati, diviso le temperature costanti a cui questi scambi avvengono. I calori assorbiti sono positivi, quelli ceduti sono negativi. In una trasformazione ciclica, ideale, la variazione di entropia è nulla. Anche l’ambiente esterno non subisce variazione di entropia quando il ciclo è reversibile;
quindi l’entropia del sistema isolato (macchina + ambiente esterno),
rimane costante: DS = 0.
Se invece in un sistema isolato avvengono trasformazioni irreversibili (reali), allora l’entropia aumenta sempre. Qualsiasi trasformazione reale lascia un segno nell’ambiente,
quindi: DS > 0.
Questa funzione di stato detta entropia è stata introdotta da Clausius (coniando la parola da un verbo greco e vuol dire “andare verso”), per esprimere il 2° principio, perché indica il verso spontaneo delle trasformazioni e l’irreversibilità del tempo, ciò che è “prima”, ciò che è “dopo”. Se pensiamo all’universo intero come un sistema isolato che non scambia energia, allora possiamo dire che per il 1° principio l’energia totale dell’universo si conserva, per il 2° principio la sua entropia tende ad aumentare. Quando l’entropia avrà raggiunto il valore massimo, non saranno più possibili scambi di energia e quindi scambi termodinamici . Questa situazione viene chiamata “morte termica dell’Universo”. L’aumento di entropia è un indice della degradazione dell’energia, che si conserva, ma non è più utilizzabile.
ORDINE DISORDINE
Un sistema evolve verso uno stato di maggior disordine, l’entropia aumenta.
Sistema disordinato. Si può ripristinare l’ordine introducendo nel sistema un lavoro.
L’energia meccanica si trasforma in calore, l’energia si degrada.
L’entropia Q/T , aumenta
Esempio di aumento di entropia: Due automobili di massa m1= 1100 kg ed m2 = 800 kg stanno viaggiando alle velocità v1=95 km/h e v2=50 km/h in direzioni opposte. Esse si scontrano e si fermano. Determinare la variazione di entropia DS dell’ universo in seguito alla collisione. Assumete che la collisione avvenga a temperature T = 20°C.
V1 = 95/3,6 =26,39 m/s
V2 = 50/3,6 = 13,89 m/s
E1 + E2 = 1/2 x 1100 x 26,39^2 + 1/2 x 800 x 13,89^2 =
= 383038 + 77161 = 4,602 x 10^5 J ( L’energia diventa calore che viene assorbito dall’ambiente, il calore assorbito è positivo).
DS = Q/T = + 4,602 x 10^5 / (20°+273) = +1571 J/K
Questo valore ci dice che l’entropia dell’universo è aumentata e che questa energia (1571 J per ogni Kelvin), non è più utilizzabile per fare lavoro meccanico. L’energia esiste ancora, ma si è “degradata”.
Esempio 2 : Una macchina termica lavora tra una sorgente fredda costituita da una miscela di acqua e ghiaccio a temperatura T1 e una sorgente a temperatura T2 = 373 K, con un rendimento η = 0,2. La massa di ghiaccio che si scioglie in un ciclo è m = 0,17 g. Determinare:
1. il calore assorbito in un ciclo dalle sorgenti;
2. la variazione di entropia delle due sorgenti;
3. il lavoro prodotto dalla macchina. ( Qfusione = 333⋅10^3J /Kg).
Calore ceduto alla sorgente fredda che si trova a temperatura
T1 = 273 K ; (t = 0°C, ghiaccio fondente)
Qced = 0,17 x 10^-3 x 333 x 10^3 = 56,61 J ( calore per fondere il ghiaccio)
(Qass – Qced)/ Qass = η
η = 0.2
Qass – Qced = η Qass
Qass = Qced/( 1 – η ) = 56,61 / ( 1 – 0,2) = 70,76 J
DS1 = Qced/T1 = + 56,61 /273 = + 0,207 J/K ( la sorgente fredda assorbe calore e aumenta l’entropia)
DS2 = Qass/T2 = – 70,76 / 373 = – 0,190 J/K ( la sorgente calda cede calore e diminuisce la sua entropia); sommando le due variazioni si vede che l’entropia aumenta
DS1 + DS2 = 0,207 – 0,190 = 0,017 J/K per ogni ciclo.
Lavoro in un ciclo:
L = Qass – Qced = 70,76 – 56,61 = 14,15 J ( per ogni ciclo).
Esercizi.
1) Una macchina di Carnot riceve nella fase di espansione una quantità di calore Q=100 J, alla temperatura di 300°C. Sapendo che la fase di compressione isoterma avviene a temperatura di 300 K, calcolare il lavoro svolto nel ciclo. L’energia cinetica diventa calore Q
h = (T2 – T1)/T2
T2 = 300°C + 273 = 573 K
T1 = 300K
h = (573 – 300) /573 = 0,48
L = h x Q = 0,48 x 100 = 48 J
Ciclo di Stirling

Il ciclo di Stirling è utilizzato per ottenere macchine termiche con rendimenti molto elevati. Esso è costitutito dalle seguenti trasformazioni:
A -B : espansione isoterma, fino a raggiungere una pressione di 6 atm
B- C: isocora fino alla pressione di 1 atm ( pressione atmosferica)
C- D: compressione isoterma , fino a ritornare al volume iniziale
D – A: isocora con i gas che ritorna nelle condizioni inizlai
A compiere il ciclo sono n = 2 moli di gas monoatomico, aventi temperatura iniziale TA = 600 K e volume iniziale VA = 4 dm^3.
– Determina i valori dei paramentri di stato ( pressione olume e temperatura) in ciascuno stato A, B C D
– determina il lavoro eseguito e energia interna per ogni trasformazione
– determina il lavoro totale
– determina il rendimento di questa macchina termica
– determina il rendimento della macchina di Carnot
PA = nRTA/VA = 2 x 0,082 x 600/4 = 24,6 atm
R è la costante dei gas = 0,082 atm x dm^3/(molK)
VA = 4 dm^3
Isoterma AB; TA = TB = 600 K
PB = 6 atm
PB x VB = PA x VA
VB = PA x VA / PB = 24,6 x 4 / 6 = 16,4 dm^3
isocora BC; volume costante VB = VC = 16,4 dm^3
PC = 1 atm
PC /TC = PB/TB; la pressione diminuisce di 6 volte, anche la Temperatura diminuisce di 6 volte.
TC = PC x TB / PB = 1 x 600 / 6 = 100 K
isoterma CD; TC = TD = 100 K costante
VD = 4 dm^3
PD x VD = PC x VC
PD = PC x VC/VD = 1 x 16,4/4 = 4,1 atm
DA isocora si ritorna alle condizioni iniziali
Lavoro: LAB = n x R x TA x ln(VB/VA); R = 8,31 Joule/molK; per avere il lavoro in Joule
LAB = 2 x 8,31 x 600 x ln(16,4/4) = 14070 J
DeltaU isoterma AB = 0 J
Lavoro delle isocore = 0 J, perché non c’è variazione di volume
DeltaU isocora BC = 3/2 R x n x (100 – 600) = – 12465 J (il gas si raffredda, cede calore)
LCD = n x R x TC x ln(4/16,4) = – 2345 J (lavoro negativo perché subìto dal gas dall’esterno, il gas viene compresso).
Lavoro totale = 14070 – 2345 = 11725 J
DeltaU isocora DA = 3/2 x R x n x ( 600 – 100) = + 12465 J ( il Gas si scalda, assorbe calore)
Q assorbito dal gas = 14070 + 12465 = 26535 J
rendimento: eta = Lutile / Qass = 11725/26535 = 0,44 = 44%
rendimento di Carnot: eta = (T2 – T1 ) / T2= (600 – 100) / 600 = 0,83 = 83%






















